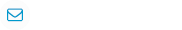遺伝子治療
がん遺伝子治療とは
全てのがんの発現には遺伝子の異常や欠如が大きく関係しています。ほとんどのがん細胞はがん抑制遺伝子が正常に機能していません。このような遺伝子の異常によりがん化した細胞に、遺伝子を正常に導く治療タンパクを投与することにより、がんの無限増殖を抑制し、アポトーシス(自然な細胞死)を促進させるのが遺伝子治療です。
がん遺伝子治療の効果を左右するのは、
①どのような多種の治療タンパク(抑制遺伝子やmRNA)を使用するか?
②がんに高濃度に治療タンパクを届ける、優れたベクター(運び屋)を使うか?
この2点が遺伝子治療の効果を決める重要なポイントです。
がん遺伝子治療も常に進化しているので、
・多種のがん抑制遺伝子やマイクロRNAなど治療薬の開発
・がん組織になるべく高濃度に治療薬を届けるドラックデリバリーシステムの開発
など開発が進んでいる医療機関を応援します。
人は約60兆個の細胞から成り立ち、増殖と自滅でバランスをとっている。
①増殖を抑制するPTENというがん抑制遺伝子
②自滅を促進するp53というがん抑制遺伝子
③老化した細胞を排除するp16というがん抑制遺伝子
これらの作用により細胞は60兆個をバランスよく維持しています。
がんは「無限増殖」「不死」の状態である。
→がん遺伝子治療はがんの原因である遺伝子異常を改善する。
Ⓐほとんどのがん組織においてがん抑制遺伝子の機能が低下している。
→がん遺伝子治療はこのようながんの原因となるがん抑制遺伝子を投与します。
p53 p16 PTEN (GATA3)
Ⓑがんにおいて増えるとよくない蛋白(がんの増殖を促進させるCDC6、がんの発現に関係するEZH2、がん抑制機能を阻害するガンキリンなど)があり、これらを作るがあり、これらを作るマイクロRNA(mRNA)が増加している。
→がん遺伝子治療はこのmRNAを抑制するRNAを投与します。
CDC6抑制RNA EZH2抑制RNA ガンキリン抑制RNA
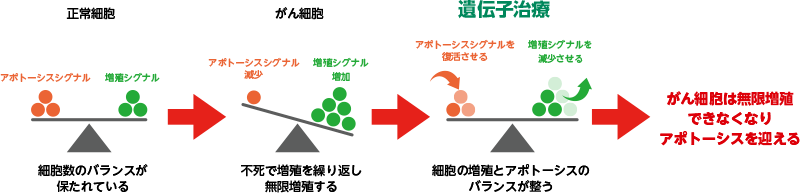
このようにがん遺伝子治療では、どんなベクターを使用し、どんな治療タンパクを持ち込み、それをどのように発現させるかが、治療効果の重要な鍵となります。
遺伝子治療はがんの種類や病期を問わず優れた効果を発揮します。がんは遺伝子の異常から発現するため、原因となっている遺伝子に直接作用する遺伝子治療がほとんどのがんに効果を示すのは当然のこととも言えます。
抗がん剤には自滅促進型と増殖抑制型(分子標的薬)があります。
自滅促進型の抗がん剤とp53・p16はDNAに対する作用機序が似ているため相乗効果を示す。
増殖抑制型の抗がん剤とPTENは同じ増殖シグナル抑制に働きかけるため相乗効果を示す。
また放射線治療に対してDNAに損傷がある細胞を自滅に追い込むp53・p16は相乗効果を示す。
がん遺伝子治療はこのように放射線治療や抗がん剤との相乗効果も非常に高く、標準治療との複合治療はより大きな効果が期待されます。
主に点滴投与による苦痛のない、副作用もほとんどない、肉体的にも精神的にも優しい有効的な治療です。
治療タンパクとベクター
がんの代表的な特徴として「不死」と「無限増殖」が挙げられます。したがってがん治療におけるポイントとして、がん細胞をアポトーシス(自然な細胞死)に導くこと、がんの増殖を止めること、この2点からがんを攻めることが大切です。がん細胞をアポトーシスに導くことと、増殖を止めることは同じようなことに思えますが、実は異なるアプローチが必要です。
従来の遺伝子治療は、がんの「不死」と「無限増殖」に対し、どちらかにしか効果の認められないものも存在していました。しかし最新のがん遺伝子治療では、がんの「不死」と「無限増殖」に対し、それぞれに効果の高い治療タンパクを使用します。
「不死」に対してp53・p16
「増殖」に対してPTEN・CDC6抑制RNA
更にはがんの「発現」という特徴に関係するEZH2を抑制するEZH2抑制RNA
そして新たに加わった「がん抑制機能の阻害」を抑制するガンキリン抑制RNA
などを用い、がんの特徴に合わせてそれぞれに働く複数の治療タンパクを組み合わせて使用しています。
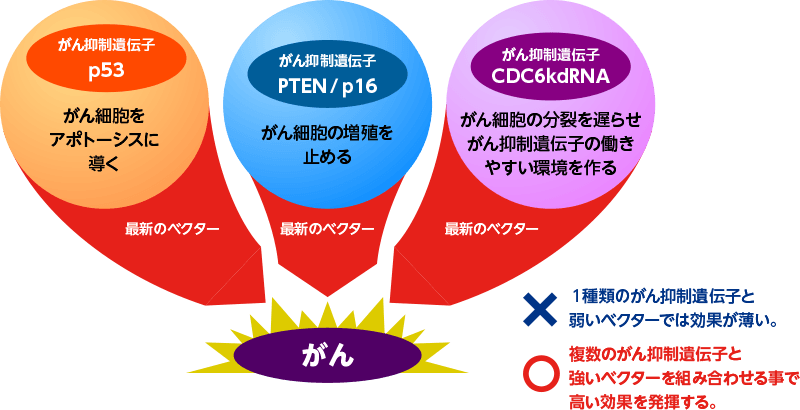
これらの治療タンパクを投与してがん組織に高率に到達させるために欠かせないのが、ベクターです。ベクターは、運び屋として治療タンパクを体内のがん細胞に届ける役割を持っています。安定してがん細胞にまで安全に届けるために、どんなベクターを使うかが非常に大切になります。
当初の遺伝子治療では、アデノウイルスというベクターを用いていましたが、発現期間が短く、細胞内に入り込む可能性も少ないため遺伝子治療のベクターとしては不十分なものでした。後に非ウイルス性で発現期間が長く、がん細胞内に半特異的に反応する特別な微小胞ベクターを使用することにより、遺伝子治療の効果は大きく前進しました。
最新の遺伝子治療では、より改良した特殊なベクターを使用しています。
①ベクターを最新の高分子ミセル化することによって、正常な血管は通過せず、粗造ながんの血管壁だけ通過する大きさ(100nm前後)に揃えています。(ドラックデリバリーシステム=DDS)
②がんや幹細胞が持っている無限に増殖できるヒトテロメラーゼ。このヒトテロメラーゼに反応するヒトテロメラーゼ逆転写酵素を付けることで半特異的にがん細胞の中で反応させる。
③特殊なベクターでがん細胞内へがん抑制遺伝子を侵入させ長期発現させる。
このように進化する有効的なベクターでがん抑制遺伝子や抑制mRNAをがん細胞に到達させています。
「p53」
p53は「ゲノムの守護神」とも言われ、生まれてから死ぬまで・つま先から頭の先まで、すべての細胞が30億の遺伝子情報を維持できるのはp53の働きによるものです。p53は細胞分裂の時DNAの修復を指示したり、DNA損傷が強い場合は細胞死(アポトーシス)を指示するなど、DNAに傷を持っている細胞を制御する機能を持っていて、細胞ががん化したときにアポトーシスさせるノーベル賞を取ったがん抑制遺伝子です。
がんと最も深い関わりのあるがん抑制遺伝子とも言われていて、がん組織内において約60%のがん患者さまに(再発の患者さまのほとんどに)p53遺伝子の変異・欠損・機能障害が認められています。
がんはこのp53の働きを抑制するためにp53と結合するMDM2というタンパクを多く産生したり、場合によってはp53に対する抗体を作り、p53が働けないように策を投じます。
なのでがん組織に単純にp53を投与してもなかなか本来の働きをしてくれません。
最新の遺伝子治療で使用するp53はMDM2やp53抗体になるべく反応しないように改良し、優れた治療効果が得られるようになりました。
p53はDNAに傷をつけるような抗がん剤(自滅促進型抗がん剤)や放射線治療と相乗効果を示します。
「PTEN」
PTENはがん組織内において約50%のがん患者さまに(再発の患者さまのほとんどに)機能障害が認められ、p53に並ぶ代表的ながん抑制遺伝子と考えられています。PTENは通常細胞の増殖シグナルを脱リン酸化により遮断して細胞増殖を停止させる。なのでPTENは特にがんの激しい増殖に最も関与しているがん抑制遺伝子である。
がん組織においてPTENの働きが阻害されると、がんの増殖シグナルを遮断できないので、がん組織において血管新生が促進され、増殖因子が多く作られがん細胞の増殖は加速されます。
PTENの投与によって、細胞の増殖シグナル経路の途中の伝達物質を脱リン酸化させることで増殖シグナルを遮断して、がん細胞の過剰な増殖を阻害します。増殖阻害された細胞はやがて細胞死を迎えます。
PTENはがん細胞の増殖シグナルを遮断することで増殖を抑制する。同じ経路で働く抗がん剤(増殖抑制型抗がん剤=分子標的薬やホルモン剤)と相乗効果を示します。
「p16」
p16は細胞老化に関係したがん抑制遺伝子で、細胞の異常な増殖を防ぎ、がんの発生を予防してくれるものなので、正常な細胞ではほとんど機能していません。しかし老化していらない細胞には細胞分裂周期中に細胞分裂を遅らせたり、異常細胞を排除したりします。
p16はがん患者さまのがん組織内において約30%に(再発の患者さまのほとんどに)機能障害が認められるがん抑制遺伝子で、特に喫煙者の肺がんなどでは高い確率で欠損しています。
p16の投与により、がんの新生血管形成が阻害されるほか、細胞分裂において一番重要な分裂期への移行のストッパーとしても働きます。また、p16は他のがん抑制遺伝子が正常に機能できる体内環境を作る役割も持っています。
p16の投与はがん細胞の増殖を抑制して自滅排除するので抗がん剤との併用で相乗効果を示します。
「CDC6抑制RNA」
CDC6は、細胞を増殖させるために働くタンパク質で、細胞の周期を調整する働きを持っています。通常は、細胞周期の初期の段階で少量のみ現れますが、ほとんどのがん細胞では周期に関わらず大量にCDC6が発現してしまい、がん細胞の増殖の元となる細胞分裂を増進します。
その結果、がん細胞が無限増殖するばかりか、がん抑制遺伝子の働きをも抑制していまいます。
CDC6は正常な細胞分裂にも存在します。CDC6は30億の遺伝情報のCDC6を作る部分があり、そこをmRNAがコピーして細胞質でCDC6を作成します。がん細胞においてCDC6の製造が増加しているので、CDC6をつくるmRNAに反応させて干渉(RNA干渉)させ、CDC6の生産を抑制させるmRNAを投与してCDC6産生を抑制する。
このmRNAに反応させて生産されるタンパクを抑制させる方法をRNA干渉といい、p53同様ノーベル賞を取りました。がん細胞は大量にCDC6を産生するので、RNA干渉を利用してCDC6の産生を抑制します。
またCDC6の抑制はp53などのがん抑制遺伝子が働きやすい環境を作ります。
「ガンキリン抑制RNA」
ガンキリン抑制RNAは がん抑制遺伝子の働きを阻害するガンキリンの産生を抑制します。
ガンキリンは、1998年に京都大学医学研究科の藤田潤教授らによって、ヒトの肝細胞がんから発見された新しいがん遺伝子(悪者)で、ほぼ全てのがんに含まれている厄介なタンパク質です。その機能は 従来がんを抑制するがん抑制遺伝子(p53、p16、PTEN、RB等)の働きを阻害します。
ガンキリンは多くのがん抑制因子を阻害するので、がん細胞の特性である「不死」や「増殖」、さらにがんの「発生」から「転移」「浸潤」に至るまで阻害し、標準治療の効果までも低下させます。ガンキリンはほとんどのがん細胞で高頻度に 高発現していることがわかっており、ガンキリンの発現が多いほど浸潤、転移が多く、予後不良であることも認められています。
「ガンキリン抑制RNA」は、ガンキリンをつくるRNAに反応させ、RNA干渉を利用してガンキリンの発現を抑えることで、がん抑制遺伝子が本来の働きを取り戻し、効率的にがん細胞の消滅を促進します。
「ガンキリン抑制RNA」は、私たちの治療タンパクを作成しているアメリカで開発され作られました。ガンキリンを抑制することで、従来の遺伝子治療がより効果的になりました。
「EZH2抑制RNA」
EZH2は、細胞を発現させるために働くタンパク質で、がん細胞などの発現にも大きく関与しています。
進行の早いがん組織ではEZH2が多量に存在します。EZH2が多く存在するがんは発現力が強く進行も速いため予後の悪いがんとなります。
この発現に関与するEZH2もCDC6同様に正常な遺伝情報からmRNAのコピーで作られます。
なのでEZH2を作るmRNAに働く、EZH2抑制RNAを投与しRNA干渉を利用してEZH2の産生を抑制します。
EZH2を抑制させることは進行の早いがんや再発予防に重要な働きをします。
現在EZH2を抑制させる抗がん剤が研究開発中である。
「その他のがんを抑制する因子の開発」
日々遺伝子治療は進化しています。がん相談窓口(GTech)でも最新のがんを抑制する因子の開発を依頼しています。
現在開発中で今後加わるものとして乳がんの特にトリプルネガティブに関係したGATA3/GATA4※がん遺伝子に働きかける遺伝子治療などを開発中です。
このようにがん遺伝子治療やがん遺伝子分析は日々進化しています。
遺伝子治療も日々進化する必要があります。
※がんはがん抑制遺伝子の機能が低下の場合とがん遺伝子からの産物による細胞増殖過多の場合がある。
現在はがん抑制遺伝子からのアプローチがほとんどです。(がん遺伝子治療や抗がん剤)
私たちはもう一つの原因であるがん遺伝子側の増殖抑制も考えている。
「最新のベクター」
非ウイルス性の特別な微小胞ベクターです。最新の研究によって、運び屋としての役割のみを追求して作り上げたものです。さらに高分子ミセル化(優秀なドラッグデリバリーシステム)と進化させ従来のベクターよりがん細胞内にさらに侵入しやすくなり、治療タンパクの効果を高めることができました。
このことより近い将来、がん遺伝子治療の経口薬を開発できる可能性も高まりました。
輸入製剤について
| 未承認医薬品等であることの明示 | 本治療に用いる遺伝子は、医薬品医療機器等法上の承認を得ていない未承認医療機器です。日本では、未承認医薬品を、医師の責任において使用することができます。 |
|---|---|
| 入手経路等の明示 | 当社で紹介している遺伝子は、米国「GANKILL PHARMA USA」社で製造されたものを、各医院様において個人輸入いただいております。この医薬品等の使用によるリスク関する情報は下記URLをご確認ください。 https://www.yakubutsu.mhlw.go.jp/individualimport/healthhazard/ |
| 国内承認医薬品等の有無の明示 | 国内においては承認されている医療機器はありません。 |
| 諸外国における安全性等に係る情報の明示 |
Germline-integrationのリスク評価 General Principles to Address the Risk of Inadvertent Germline Integration of Gene Therapy Vectors Oct. 2006 |
最新の遺伝子治療
「有効多種の治療タンパク」
がんには「無限増殖」「不死」をはじめ、さまざまな特徴(発現や抑制遺伝子への阻害など)があるため、単一のがん抑制遺伝子や治療タンパクでは得られる効果に疑問が残ります。また状況にあったオリジナルな遺伝子治療が必要になります。
実際に多くの患者さまにCTC検査(末梢循環腫瘍細胞Circulating Tumor Cell)で調べてみると(浸潤・転移・血管新生・増殖シグナル・受容体・細胞周期・不死など)多種にわたり障害を受けている。
したがって治療においてもがん細胞の増殖を抑える、アポトーシスに導くなど、複数のがん抑制遺伝子やmRNAを用いて、多角的にアプローチする必要があります。
また、がん抑制遺伝子をがん細胞まで運ぶベクターの働きも重要です。がん細胞内まで入り込めないベクターや発現期間の短いベクターでは、がん抑制遺伝子が十分に働くことができません。大きさも重要でしっかりしたドラッグデリバリーシステム(DDS)を持つことが重要です。EPR効果(腫瘍に対して高濃度でより多く、そして長く保持させる効果)を上げる努力が大切です。
p53は非常に重要ながん抑制遺伝子ですが、多くのがん組織でp53の働きを抑制するp53抗体や多量のMDM2そしてガンキリンなどが存在するため、そのままではp53が阻害されてしまい十分な効果が得られません。p53の機能低下は抗がん剤や放射線治療の効果を下げてしまいます。
MDM2やp53抗体に反応しにくいp53を用いることが、標準治療やがん遺伝子治療の重要な鍵となります。
更にガンキリン抑制RNAを追加することで、p53をはじめとする主要ながん抑制遺伝子がより働きやすい環境となり、がん抑制遺伝子の機能が十分に発揮されます。
「がん細胞に有効的に到達させる努力」
私たちが提供するがん遺伝子治療は最新型がん遺伝子治療です。この開発は現在も日々進化を続けています。藤田潤先生との共同作業により、今回はガンキリン抑制RNAも登場しました。
このように我々は日々がん遺伝子治療がより有効になるように進化しています。遺伝子治療薬を運ぶベクターも多くのベクターを使用して、より効果が出るように進化しています。現在は高分子ミセル化して、大きさを100nm前後にして、完全に病原性を排除し、がん細胞内にまで入り込む発現期間が長いものを使用しています。
私たちのがん遺伝子治療は腎臓から排泄されにくく、3~5日ぐらい体を循環してがん組織を探します。
①高分子ミセル化
正常な血管は通過せず、粗造ながん血管壁だけ通過する大きさ(80nm~100nm前後)に整えて、がん到達率を高める。(ドラックデリバリーシステム=DDS)
この大きさにすることを高分子ミセル化といい、現在抗がん剤もこの大きさに変える研究中です。
これによりがんに高率に入り、副作用が少ない抗がん剤ができる。
②ヒトテロメラーゼ逆転写酵素(h-TERT)を利用
細胞分裂の時DNAの転写はテロメアという部分から始められる。テロメアは分裂するたびに削られていき、無くなったら細胞は死を迎える。なのでテロメアは「細胞の死の回数券」ともいわれる。
しかしがん細胞や幹細胞は、無限にテロメアを作るヒトテロメラーゼという酵素を持っている。がんや幹細胞はこのテロメラーゼにより無限にテロメアを作ることができるので、無限に分裂することができる。
この特徴を利用してヒトテロメラーゼ逆転写酵素(h-TERT)を付けることで、がん細胞の中で大きく反応する。h-TERTにより、がん細胞に対して半特異的に反応させる。
③特別な微小胞ベクター
がん細胞内に長く留まり半特異的に反応する非ウイルス性の特別な微小胞ベクターの開発に成功しました。このことによりがん抑制遺伝子をがん細胞内に高率に運び込み、長期発現することができます。
つまり高分子ミセル化でがんに寄せ、h-TERTでがん細胞に半特異的に反応させ、特別な微小胞ベクターによってがん抑制遺伝子を届ける。
がん遺伝子治療の優れた特徴
1. 副作用が少なく軽い
副作用として発熱や頭痛や血圧変動が起こる場合がありますが、解熱剤やごく少量のステロイドを投与することで、副作用はほぼ抑えることができます。
またアナフィラキシーショックの発生率は0.3%(軽い反応のみ)以下です。
副作用が少ないので発がん予防・再発予防・再発中・末期まで使用可能です。
2. 正常細胞に影響を与えない
治療で使用するがん抑制遺伝子は正常細胞にもともと備わっている遺伝子ですので、投与することで正常細胞へ影響を与えることはありません。
3. 抗がん剤や放射線治療の効果を増強させる
抗がん剤治療や放射線治療は、細胞分裂の際にDNAを損傷または転写阻害して細胞死に追い込みます。遺伝子治療もDNAが損傷された細胞を排除するので、抗がん剤や放射線治療の効果を増強させることができます。また分子標的薬の増殖阻止とPTENは同じ経路で働くため相乗効果を示す。
また抗がん剤に対する耐性がん細胞にも有効なので併用により相乗効果を示す。
4. 細胞レベルでもがんに対処
遺伝子治療の効果は血管やリンパ管から全身の細胞に広がりますので、転移の恐れがある手術前から手術後の再発予防にも有効となります。また早期がんも再発することがあります。抗がん剤を使わないがんの治療にも細胞レベルで全身に広がるがん遺伝子治療は有効です。
5. 前がん状態にも対処
まだがんを発症していなくても、がん抑制遺伝子が正常に機能していない前がん状態の細胞も同様に作用するので、前がん状態の細胞の増殖を止めたり、自滅に追い込むことができます。
がん発現の予防にも効果的です。
6. 耐性にならない
抗がん剤は、初めから効き難い薬剤自然耐性と使用し続けることで効き難くなる薬剤獲得耐性があります。前者はもともと抗がん剤に強いがん細胞でがん幹細胞やストレスに強い細胞がある。
後者は抗がん剤自体が細胞毒である薬剤耐性遺伝子が働くことで耐性を獲得する。
しかし遺伝子治療はウイルスのかけらを使うので、直接がん細胞内に入り作用するので、耐性ができ効果が得られなくなることなく、長期使用が可能である。
7. がん幹細胞や難治性のがんにも有効
抗がん剤や放射線が効きにくい、がん幹細胞やストレスに強いがん細胞。抗がん剤から打ち勝ってきて増殖した難治性の再発がんにも直接がん細胞内に入り込むがん遺伝子治療は効果を現す。有効的な相乗効果を利用した、標準治療+遺伝子治療(複合医療)をすることにより、治療効果が飛躍的に上がります。
8. 治療適応範囲が広い
抗がん剤・放射線治療・免疫療法など、どのがん治療とも相乗効果を示し併用が可能である。またがんの予防・再発予防、再発がん治療、末期がんの延命など、がんの病期を問わず有効です。強い副作用がないので、体力の衰えの激しい患者さまでも、仕事をしながらでも治療が可能です。
9. がんの種類を問わない
がんの原因は遺伝子異常。がん遺伝子治療はがん細胞の変異した遺伝子をターゲットとします。がん遺伝子治療は異常遺伝子に直接作用するため、がんの種類や部位を問わず、どのがんでも有効です。また抗がん剤が効きにくい、ストレスに強いがん細胞やがん幹細胞や難治性のがんにも効果が期待できます。
10. 場所を選ばない
通常の治療方法は点滴投与となります。がん腫瘍へ直接注入する方法も可能です。比較的簡単な治療なので、入院や特別な施設、装置は必要ありません。
がん発現予防と再発予防
従来はがんを積極的に予防することは現実的とは言えませんでした。しかし、がん遺伝子治療によってその可能性は大きく広がりました。
標準治療は、がんが発見されてからの対応になりますが、遺伝子治療は前がん状態に対しても非常に高い有効性を示します。遺伝子治療には副作用がほとんどありません。正常細胞に悪影響を及ぼすことなくがん細胞を攻撃するので、健康な方が受けたとしても全く問題ありません。遺伝子治療は、がんになる前の予防として使うことも可能なのです。また比較的軽い癌は身体に副作用が起こる抗がん剤は使いません。しかしこのようながんでも再発することはあります。このような時も副作用がほとんどないがん遺伝子治療は有効な治療法です。
まだPET-CTなどの画像検査で発見できないような前がん状態があったとしても、発がんと言える大きさになる前に消し去ってくれる可能性もあります。
画像検査で発見できるかもしれない5ミリ程度の大きさに成るまでには何年もの時間を要します。この発がんと呼ばれる状態になる前に 予防的に遺伝子治療を受けることで発がんを防ぐ可能性が高くなります。
がん遺伝子治療は、人間がもともと持っているがんを発生させないための仕組みである、がん抑制遺伝子を利用した治療法ですので、副作用もほとんどなく、全身のどこにあるかもわからないがん細胞を攻撃することが可能なのです。がんと診断される前に治療する、まさに究極のがん治療とも言えるでしょう。
また、三大標準治療だけでがんの再発を防げる可能性は決して高くありません。しかし標準治療に、遺伝子治療を加えることにより再発を防ぐ確率が向上します。
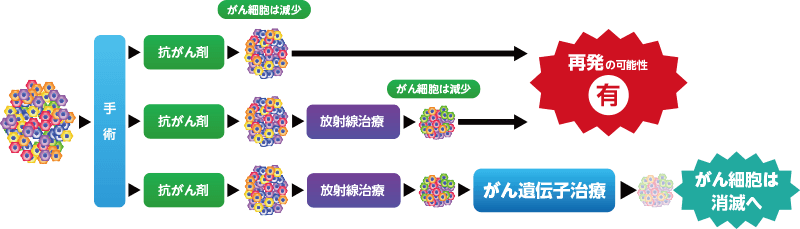
がんは、一定の治療を終えたとしても細胞レベルで存在しているケースが多くあります。そのまま何もしなければ再発の可能性は非常に高くなります。標準治療では再発予防として抗がん剤を使用することも多いですが、十分な再発予防になるとは言えません。なぜなら抗がん剤には副作用と薬剤耐性という問題があるため、全身のがん細胞を確実に消滅させる可能性が高いとは言えないからです。
しかし標準治療はここで治療を終えるしかありません。結果的にほとんどの患者さまは、「再発するかもしれない」状態で治療を終えてしまいます。
この「再発するかもしれない」状態は、実は再発を防ぐために最も大切な時期なのです。がん細胞が体内に残っていたとしても、その数と勢いが最も弱まっているこのタイミングこそが、再発予防にとって最大のチャンスです。がん再発を防ぐために最も効果的なのは「複合治療」です。
例えば手術が適応になる患者さまであれば、手術後になるべく早く一番効果ある抗がん剤を投与して、必要であればそれに放射線治療を追加、そしてがん遺伝子治療を加える。これががん治療にとって最高に効果ある、もっとも再発率を下げる「複合治療」だと言えます。
がん遺伝子治療は三大標準治療の効果をより高めるばかりでなく、正常細胞に影響なくがん細胞にのみ効果を表すため副作用がほとんどありません。さらにどこに存在するかわからない全身のがん細胞にも遺伝子レベルで作用するため、再発予防としては最適と言えます。さらに遺伝子治療と免疫療法を組み合わせると、免疫のがん細胞に対する感作力が高まるため、より強力に再発を防ぐことが可能です。
遺伝子治療の副作用
がん遺伝子治療は抗がん剤のような強い副作用はありません。
また、治療タンパクを使用するため、アレルギー反応やアナフィラキシーショックがごく稀(0.3%)に起こる可能性がありますが、事前にアレルギー反応テストを行い、安全を確認した後に治療を開始しますのでほとんどの例が軽症で終わります。
治療タンパクは、がん到達率を高める(EPR効果)ため、高分子ミセル化した優れたドラッグデリバリーシステム(DDS)を利用しています。この高分子ミセル化に対し考えられる副作用としては、体内血流増加(ABC)現象が起こることが時々あるので、頭重感、頭痛、微熱といった症状がでる場合があります。
発生率としては15%程度となり、この様な症状がでた場合には、軽い痛み止め(解熱鎮痛剤)を服用することですぐに改善します。
またがん遺伝子治療の弱点は免疫療法と同じように投与できる安全域の量が決まっていることです。
がん遺伝子治療 費用の目安
がん遺伝子治療は自由診療となるため、公的保険は適用されません。
治療費は患者様のご状態などにもよりますので、詳しくはお電話でご連絡の上、インフォームドコンセントをお受けください。(TEL:0120-881-888)
インフォームド・コンセント(セカンドオピニオンも可能)費用 / ¥5,500(税込)
インフォームドコンセントは、患者様のご状態をより詳しくお伺いするためにも、2時間程度のお時間をいただいております。
がんと診断され手術ができない方、再発された方(体内にがんが存在)
がん治療
| 1クール目(点滴6回) | 治療技術料+治療たんぱく費¥176,000~¥319,000(税込) |
|---|---|
| 2クール目(点滴5回) | 治療技術料+治療たんぱく費¥176,000~¥319,000(税込) |
1クール一括払いでは無く、治療1投与ごとの都度払いになります。
投与毎に一般血液検査や腫瘍マーカーなどを計り、画像診断なども考慮して治療効果の判定を行っております。
尚、一般血液検査の費用は、治療技術料に含まれております。
再発を予防されたい方(体内にがんがない方・手術前の方・発がん予防の方)
再発予防
| 1クール目(点滴6回) | 治療技術料+治療たんぱく費¥143,000~¥269,500(税込) |
|---|---|
| 2クール目(点滴5回) | 治療技術料+治療たんぱく費¥143,000~¥269,500(税込) |
1クール一括払いでは無く、治療1投与ごとの都度払いになります。
投与毎に一般血液検査や腫瘍マーカーなどを計り、画像診断なども考慮して治療効果の判定を行っております。
尚、一般血液検査の費用は、治療技術料に含まれております。
患者さまのご希望によって治療法を変更されたい場合や、治療を中止せざるを得ない場合など、あらゆる状況を想定し、対応できるお支払いシステムとなっております。
投与毎に一般血液検査や腫瘍マーカーなどを計り、画像診断なども考慮して治療効果の判定を行っております。
一般血液検査や腫瘍マーカーなどの費用は、治療技術料に含む医療機関と含まない医療機関があります。